Tillverkningen av oralt upplösande filmer utförs med olika metoder såsom gjutning av lösningsmedel, smält-extrudering, halvfast gjutning, extrudering av fast dispersion och valsning. Författarna diskuterar dessa metoder och de olika parametrarna där upplösande filmer utvärderas.
Jan 02, 2011
Av Pharma Technology Editors
Farmaceutisk teknologi
Volym 35, nummer 1
Orala tunna filmer eller orala upplösningsfilmer (ODF) ger snabb frisättning av en aktiv farmaceutisk ingrediens (API) när de placeras på tungan. ODF: er ger ett alternativ till oralt sönderfallande tabletter. Dessa doseringsformer placeras på en patientens' s tunga eller någon oral slemhinnevävnad. När den är våt med saliv hydratiserar filmen snabbt och fästs på appliceringsstället. Det sönderdelas snabbt och upplöses för att frisätta läkemedlet för slemhinneabsorption eller med modifieringar möjliggör oral absorption av mag-tarmkanalen med snabbupplösande egenskaper. Dessa filmer lanserades inledningsvis som munfräschande produkter innehållande ingredienser som mentol och tymol. Dessa filmer finns tillgängliga som pustfräscha produkter från Johnson& Johnson (New Brunswick, NJ) och Wrigley (Chicago) i USA och Europa och Boots (Nottingham) i Storbritannien. Zengen (Woodland Hills, Kalifornien) producerar en kloraseptisk lättnadsremsa i USA för att leverera bensokain, ett lokalbedövningsmedel för att behandla ont i halsen.
Dessa ODF innehåller filmbildande polymerer såsom hydroxipropylmetylcellulosa (HPMC), hydroxipropylcellulosa (HPC), pullulan, karboximetylcellulosa (CMC), pektin, stärkelse, polyvinylacetat (PVA) och natriumalginat. Ytterligare ingredienser som införlivas inkluderar mjukgörare, sötnings- och smakämnen, färgämnen, salivstimulerande medel och förtjockningsmedel. Lämpliga användningar för snabb upplösande filmer är nikotinersättande transdermal tillförsel, och som antiulceringsmedel och antihistaminläkemedel. Antipsykotiska läkemedel och sömnstörningar är också potentiella kandidater för receptbelagda produkter ({{4}} - 4). Fördelarna med ODF: er inkluderar förbättrad portabilitet, enkel administrering, noggrann dosering, kostnadseffektivitet och förbättrad efterlevnad av patienten.
Tillverkning av ODF: er
En eller en kombination av följande process kan användas vid tillverkning av ODF: lösningsmedelgjutning, halvfast gjutning, hot-melt extrusion (HME), solid-dispersion extrusion och rullande (1, 4 ). De mest använda metoderna för filmtillverkning är lösningsmedelsgjutning och HME.
Metod för gjutning av lösningsmedel. ODF formuleras företrädesvis med användning av lösningsmedelsgjutningsmetoden, varigenom de vattenlösliga ingredienserna upplöses för att bilda en klar, viskös lösning. API och andra medel upplöses i mindre mängder i lösningen och kombineras med bulkläkemedlet. Denna blandning sättes till den vattenhaltiga, viskösa lösningen. Den infångade luften avlägsnas genom vakuum. Avluftning är nödvändig för att erhålla enhetlig filmegenskap och tjocklek. Den resulterande lösningen gjutes som en film, får torka och skärs i bitar till önskad storlek. API: s egenskaper spelar en avgörande roll i valet av ett lämpligt lösningsmedel. API: s fysisk-kemiska egenskaper bör beaktas. Dessa egenskaper inkluderar API: s förenlighet med andra filmbildande hjälpämnen, kompatibilitet med lösningsmedel, den polymorfa naturen hos den valda API och temperaturkänslighet. Tillverkning och förpackning av ODF: er kräver särskild försiktighet för att kontrollera effekten av fukt. Bild {{4}} visar kritiska faktorer som är involverade i ODF-tillverkning med metoden för gjutning av lösningsmedel. Filmens stabilitet och dess mekaniska egenskaper påverkas avsevärt av närvaron av fukt. En annan faktor som kräver strikt kontroll är temperaturen. Kontrollerade temperaturförhållanden krävs för att bibehålla lösningens viskositet och temperaturkänsligheten i API (4).
Specifika typer av utrustning såsom rullar krävs för att hälla lösningen på en inert bas. Avståndet mellan rullen och underlaget bestämmer filmens erforderliga tjocklek. Det sista steget, torkning av filmen, tar bort lösningsmedlet och hjälper till att erhålla den färdiga produkten. Vanligtvis används glas-, plast- eller teflonplattor som en inert bas för filmgjutning. När tillverkningstekniken överförs från laboratorieskala till produktionsskala kan flera problem uppstå. Dessa problem kan innefatta gjutning av filmen, erhållande av jämn tjocklek på filmen och korrekt torkning av provet. Valet av rätt typ av torkare behövs i det sista torksteget.
När filmerna har torkats är klippning, strippning och förpackning klar. Lämplig storlek och form på filmer kan skäras. De vanligt tillgängliga storleken på filmer är 3 x 2 cm {{2}} och 2 x 2 cm 2. Val av förpackningsbehållare är en lika viktig parameter för ODF. Förpackningsbehållaren bör ge tillräcklig mekanisk hållfasthet för att skydda filmen under transport och från yttre faktorer som temperatur och fuktighet. Beroende på filmens karaktäristika kan behållare med en enhet och flera enheter vara valda. De förpackade filmerna inspekteras innan de förpackas i en sekundär förpackningsbehållare (4).
Varmsmält-extrudering. HME används vanligtvis för framställning av granuler, tabletter med fördröjd frisättning och transdermala och transmukosala läkemedelsleveranssystem (5). HME-processen har nyligen vunnit popularitet inom läkemedelsindustrin. Baserat på kunskap från plastindustrin kan formulatorer strängspruta kombinationer av läkemedel, polymerer och mjukgörare till olika slutliga former för att uppnå önskade läkemedelsfrisläppsprofiler (5). Bearbetning av filmer med denna teknik involverar formning av en polymer till en film via uppvärmningsprocessen snarare än genom den traditionella lösningsmedelsgjutningsmetoden (4).
Fördelarna med HME för filmbildning inkluderar följande:
· Du behöver inte använda lösningsmedel eller vatten
· Färre behandlingssteg
· Kompressibilitetsegenskaperna för API är kanske inte av betydelse
· Bra spridningsmekanism för dåligt lösliga läkemedel
· Mer enhetlig spridning av de fina partiklarna på grund av intensiv blandning och omrörning
· Mindre energi jämfört med högskjuvningsmetoder
· Minsta produktavfall
· Möjlighet till uppskalning
· Bra kontroll av driftsparametrar.
I HME-processen blandas API och andra hjälpämnen i torrt tillstånd, uppvärmningsprocessen startas och den smälta massan strängsprutas ut från smält-extrudern. Fördelen med denna process är fullständig eliminering av lösningsmedlet. Filmerna får svalna och skärs till önskad storlek. Den höga temperaturen som används i processen gör den lämplig för termostabila läkemedel. Läkemedel som är känsliga för temperatur kan inte användas i denna process.
Tabell I jämför lösningsmedelsgjutning och HME för tillverkning av ODF. Gjutning av lösningsmedel är en vattenhaltig process som är lämplig för termolabila och termostabila läkemedel jämfört med HME, som är vattenfri och kräver termostabila läkemedel. Repka et al. studerade påverkan av klorfeniraminmaleat (CPM) på topiska HPC-filmer av HME (5). CPM har rapporterats fungera som ett effektivt mjukningsmedel och därmed öka procentuell töjning och minska draghållfastheten på ett koncentrationsberoende sätt. CPM fungerar också som ett bearbetningshjälpmedel för extrudering av smältfilmer genom att tillåta filmbearbetning vid lägre temperaturer (6).
En utvärdering av HME och bioadhesiva egenskaper in vivo hos HPC-filmer innehållande sju polymertillsatser på epidermis hos humana individer utfördes (7). HPC-filmer innehållande tillsatser med och utan mjukgörare framställdes av HME. Införlivandet av en karbomer (Carbopol 9 7 1P NF, Lubrizol, Cleveland, OH) och polykarbofil i HPC-filmer ökade bioadhesionen avsevärt. Många studier genomfördes med användning av HME för framställning av fasta dispersioner. Det rapporterades att smältekstrudering av blandbara komponenter resulterade i amorf fast bildning av fast lösning, medan strängsprutning av en oblandbar komponent ledde till det amorfa läkemedlet dispergerat i ett kristallint hjälpämne (8). Förfarandet har varit användbart vid framställning av fasta dispersioner i ett enda steg. En extruder består av två distinkta delar. Den första delen består av ett transportörssystem som transporterar materialet och ger en grad av distribuerande blandning. En andra del, ett färgämnesystem, bildar materialen till önskad form. Läkemedelsbärarblandningen fylls i tratten och transporteras, blandas och smälts av extrudern. Formen formar smältan i den erforderliga formen, såsom granuler, pellets, filmer eller pulver, som kan bearbetas ytterligare till konventionella tabletter eller kapslar. Syre och fukt bör elimineras fullständigt för ämnen som är mottagliga för oxidation och hydrolys (9).
Halvfast gjutning. I halvfastgjutningsmetoden framställs en lösning av den vattenlösliga, filmbildande polymeren. Den resulterande lösningen sättes till en lösning av sur olöslig polymer (t.ex. cellulosaacetatftalat och cellulosaacetatbutyrat), som tidigare framställts i ammonium eller natriumhydroxid. Den lämpliga mängden mjukgörare tillsätts för att erhålla en gelmassa. Den beredda gelmassan gjuts i filmer eller band med användning av en kontrollerad värmekälla. Filmens tjocklek styrs mellan 0. 015 - 0. 05 in. (9).
Ekstrudering av fast dispersion. Termen fast dispersion hänför sig till dispersionen av en eller flera API: er i en inert bärare i fast tillstånd i närvaro av amorfa hydrofila polymerer med användning av metoder såsom HME. Vid extrudering av fast dispersion extruderas oblandbara komponenter med läkemedel och fasta dispersioner framställs. De fasta dispersionerna formas till filmer med hjälp av matriser. Läkemedlet löses i ett lämpligt flytande lösningsmedel. Denna lösning införlivas i smältan av polyoler, såsom polyetylenglykol, erhållen under 70 ° C, utan att det flytande lösningsmedlet avlägsnas. Det valda lösningsmedlet eller det upplösta läkemedlet kanske inte är blandbart med smältan av polyetylenglykolen. Den polymorfa formen av läkemedlet som fälls ut i den fasta dispersionen kan påverkas av det använda flytande lösningsmedlet (9, 10).
Rullande metod. I rullningsmetoden rullas en lösning eller suspension innehållande läkemedlet på en bärare. Lösningsmedlet är huvudsakligen vatten och en blandning av vatten och alkohol. Filmen torkas på rullarna och skärs i önskad storlek och form. Filmen är gjord genom att förbereda en förblandning och lägga till API, och filmen bildas därefter (11). Förblandningen eller master-satsen som innehåller den filmbildande polymeren, det polära lösningsmedlet och andra hjälpämnen, med undantag av API, tillsätts till master-batch-matningstanken. En förutbestämd mängd av huvudsatsen styrs och matas genom en doseringspump och styrventil till blandarna. Den erforderliga mängden läkemedel sättes till den önskade blandaren genom en öppning. Efter att API har blandats med masterbatch för att tillhandahålla en enhetlig matris matas matrisen till pannan med doseringspumpar. Filmens tjocklek styrs med en doseringsrulle. Filmen formas slutligen på underlaget och transporteras bort via stödvalsen. Den våta filmen torkas med kontrollerad botttorkning, företrädesvis i frånvaro av yttre luftströmmar eller värme på filmens yta.
Utvärdering av ODF
ODF utvärderas med olika parametrar såsom tjocklek, filmens mekaniska egenskaper, vikningsuthållighet, analys / läkemedelsinnehåll samt genom studier av in vitro-sönderdelning, in-vitro upplösning, ytmorfologi och smak ({{2 }}, 13).
Tjocklek. Bandets tjocklek kan mätas med en mikrometer på olika platser. Denna mätning är väsentlig för att fastställa enhetlighet i filmens tjocklek, eftersom denna tjocklek är direkt relaterad till noggrannheten hos dosen i remsan.
Filmens mekaniska egenskaper. De mekaniska egenskaperna är draghållfasthet, procentuell töjning och elastisk modul.
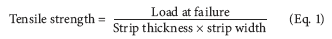
Brottgräns. Draghållfasthet är den maximala spänningen som appliceras på en punkt där remsprovet bryts. Det beräknas med den applicerade belastningen vid brott dividerad med tvärsnittsarean för remsan som anges i ekvationen nedan:
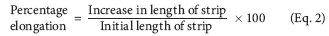
Procentuell förlängning. När stress appliceras sträcker sig ett filmprov, och denna spänning benämns belastning. Strain är i grunden deformationen av filmen dividerad med provets ursprungliga dimension. När mjukningsmedelsinnehållet ökar observeras filmförlängningen.
Rivmotstånd. En plastfilms rivmotstånd är en komplex funktion av dess ultimata motstånd mot brott. En mycket låg belastning på 51 mm / min används. Den är utformad för att mäta kraften för att initiera rivning. Den maximala spänningen eller kraften (som vanligtvis finns nära början av rivning) som krävs för att riva provet registreras som rivmotståndet i newton.
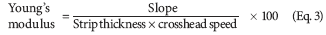
Ung' s modul eller elastisk modul. Young' s modulus eller elasticitetsmodul är måttet på filmens styvhet. Det representeras som förhållandet applicerad spänning dividerat med belastningen i området för elastisk deformation:
Hårda och spröda remsor visar en hög draghållfasthet och Young' s modul med mindre procentuell töjning.
Fällbar uthållighet. Fällbar uthållighet bestäms genom upprepad vikning av filmen på samma plats tills filmen går sönder. Antalet gånger filmen viks utan att bryta beräknas som det vikbara uthållighetsvärdet.
Analys / läkemedelsinnehåll. Analys / läkemedelsinnehåll bestäms med vilken standardmetod som beskrivs för det specifika API i någon av farmakopéerna.
In vitro-sönderdelning. Sönderfallstid ger en indikation om filmens sönderdelningskaraktäristik och upplösningsegenskaper. För denna studie placerades filmen, enligt de dimensioner som krävs för dosleverans, på ett trådnät av rostfritt stål innehållande 10 ml destillerat vatten. Den tid som krävdes för att filmen skulle bryta noterades som in vitro-sönderdelningstid.
In-vitro upplösning. In-vitro-upplösningsstudier kan utföras med användning av modifieringar av standardkorg eller paddelapparat som beskrivs i någon av farmakopéerna eftersom en konventionell paddelapparat kan leda till flytande av filmen. Lösningsmediet väljs enligt diskbänkningsförhållandena och den högsta dosen av API: n.
Ytmorfologi. En studie av ytmorfologin hos ODF utförs med hjälp av miljöskanningselektronmikroskopimetoden. Filmens enhetlighet och frånvaron av porer och striationer indikerar ODF: s goda kvalitet.
Smakutvärdering. En smakutvärderingsstudie kan utföras med hjälp av en panel med mänskliga frivilliga. ODF bör ha den önskade sötma och smak som är acceptabel för patienten. In vitro-metoder som använder smakssensorer, en speciellt konstruerad apparat och frisättning av läkemedel med modifierade farmakopémetoder används för detta ändamål. Experiment med användning av elektroniska tungmätningar har också rapporterats för att skilja mellan söthetsnivåerna i formulering med smakmaskning.
Klinisk och myndighetskrav
För att indikera bioekvivalensen hos en produkt till den för befintligt oralt läkemedel krävs en förkortad ny läkemedelsapplikation. In vitro-upplösningsstudier och terapeutisk ekvivalens beaktas. Jämförande bioekvivalens mellan en oralt sönderfallande tablett och en ODF kan utvärderas. Om ODF uppvisar en annan mål farmakokinetisk profil jämfört med den befintliga marknadsförda produkten, betraktas ODF som en ny doseringsform. För en ny doseringsform krävs en ny klinisk studie. En ny klinisk studie erbjuder fördelen med tre års marknadseksklusivitet för produkten. Prekliniska toxicitetsstudier krävs inte om molekylen är densamma som den för den godkända produkten. Säkerhets-, tolerabilitets- och effektivitetsfunktioner ska demonstreras i sådana studier. Oral slemhinneirritationstest utförs i både djurmodeller och människor. Hamster-kind-påsen är den lämpligaste modellen för att förutsäga irritationskriterier innan testning hos människor (12).
Slutsats
ODF är en möjlig alternativ dosform till oralt sönderfallande tabletter. Dessa filmer erbjuder fördelarna med trevlig munkänsla och snabb upplösning i munnen. Lösningsmedelsgjutning, varmsmält-extrudering, halvfast gjutning, fast-spridningsextrudering och valsning är viktiga tillverkningsmetoder för att producera dessa filmer.
Renuka Mishra* is an assistant professor, and Avani Amin is a professor in the Department of Pharmaceutics and Pharmaceutical Technology, the Institute of Pharmacy, Nirma University, Ahmedabad, Gujarat, India, Sarkhej-Gandhinagar Highway, Ahmedabad, Gujarat, India, renukasharma81@rediffmail.com
* Till vilken all korrespondens bör riktas.
referenser
1. S. Borsadia, D. O' Halloran och JL Osborne, Drug Del. Tech. 3 (3), 6 3 - {{5} } (200 3).
2. T. Ghosh och W.Pfister," Intraoral Delivery Systems: En översikt, aktuell status och framtida trender," i läkemedelsleverans till munhålan: Molecules to Market, T. Ghosh och W. Pfister, Eds. (Taylor& Francis, Florida, CRC Press, 2 005), sid. 1 - 34.
3. PV Arnum," Outsourcing Fast Dosage Manufacturing," Pharm. Technol. 3 0 (6), 44 - 52 (200 6).
4. R. Mishra och A. Amin, Pharm. Technol. Eur 19 (10), 35 -. 39 (2007).
5. M. Repka et al.," Hot Melt Extrusion," i Encyclopedia of Pharmaceutical Technology, J. Swarbrick och J. Boylan, Eds. (Marcel Dekker Inc., New York, volym 2, 2 n upplagan, 2 002), sid. 1488 - 1 5 04.
6. MA Repka och JW McGinity, Pharm. Dev. Technol. 6 (3), 297 - 3 04 (2001).
7. M. Repka och JW McGinity, J. Controlled Release 7 6 (3), 3 41 - 3 51 (2001).
8. J. Breitenbach, Eur. J. Pharm. Biopharm 54 (2), 107 -. 117 (2 00 2).
9. A. Arya et al., Int. J. Chem. Tech. Forskning {{1}} (1), 578 - 583 (20 1 0).
10. Gole et al.," Farmaceutiska och andra doseringsformer," USA: s patent 5648093, juli 1997.
11. RK Yang et al.," Thin Film with Non-Self Aggregating Uniform Heterogenity and Drug Delivery Systems Made Fromfr," US Patent Application 20080226695.
12. R. Mishra och A. Amin, Pharm. Technol 33 (2), 48 -. 56 (2 009).
13. RP Dixit, SP Puthli, J. Controlled Release 13 9 (2), 94 - 107 (2 009).

